Lekarze mówili jedno, pacjenci czuli drugie. Tajemnica wpływu statyn na mięśnie wyjaśniona

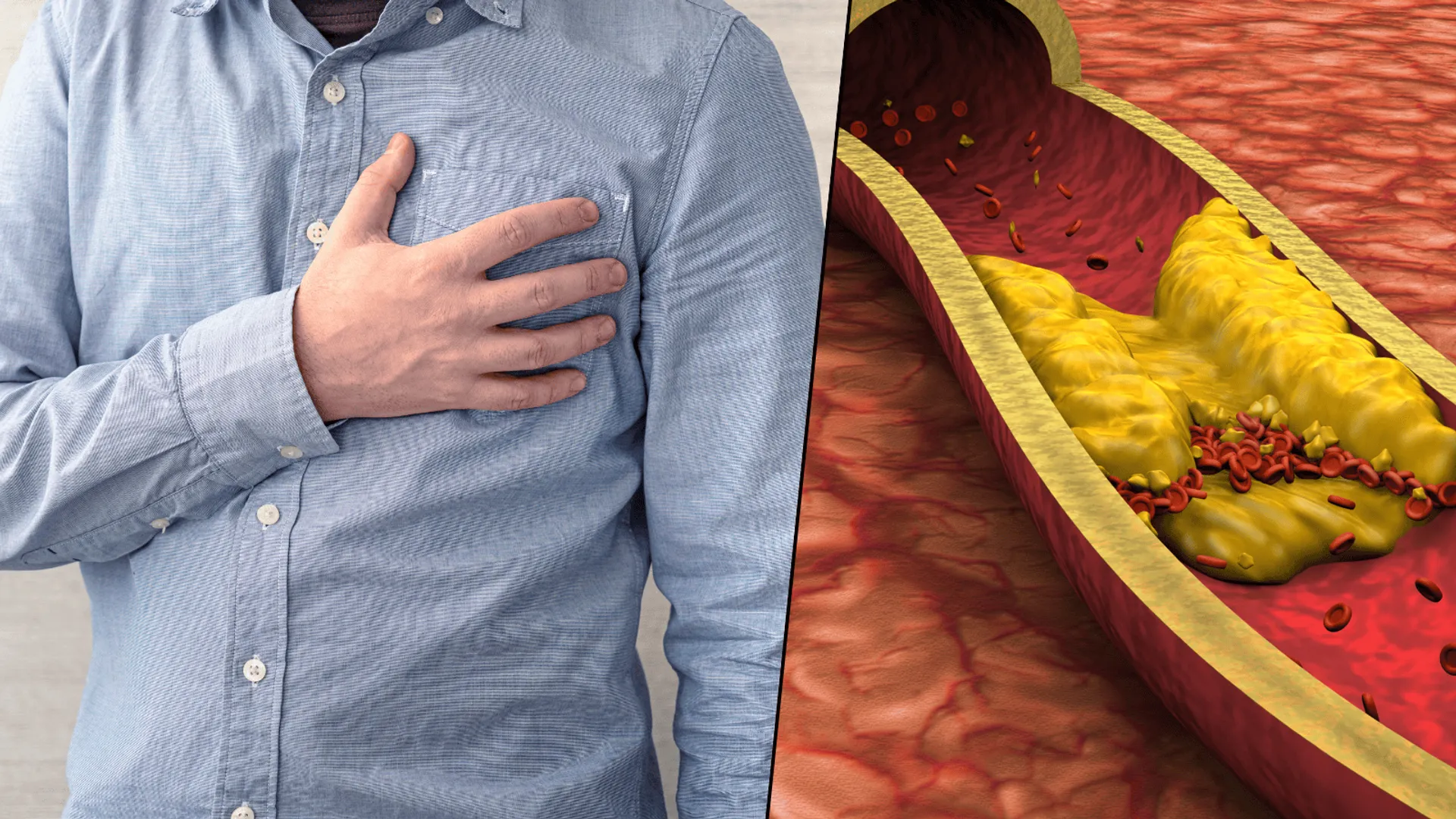
Przez dekady miliony pacjentów przyjmujących statyny zmagały się z uciążliwymi bólami mięśniowymi, które dla wielu stanowiły barierę nie do przejścia w profilaktyce chorób układu krążenia. Choć medycyna od dawna obserwowała to zjawisko, przyczyna dolegliwości pozostawała nieuchwytna, budząc frustrację zarówno chorych, jak i lekarzy. Najnowsze odkrycia naukowców rzucają jednak zupełnie nowe światło na ten problem, wyjaśniając biologiczną zagadkę, która przez lata dzieliła środowisko medyczne.
Zagadka bólów mięśniowych i ich wpływ na terapię
Dolegliwości mięśniowe towarzyszące przyjmowaniu statyn przez lata pozostawały zagadką kliniczną, mimo ich powszechnego występowania. Pacjenci najczęściej skarżą się na bóle mięśni, osłabienie oraz przewlekłe zmęczenie, co stanowi jedną z głównych przyczyn przerywania terapii obniżającej poziom cholesterolu. Choć skala problemu jest znacząca, mechanizm ten może nie dotyczyć każdego pacjenta doświadczającego skutków ubocznych.
Główne symptomy zgłaszane przez osoby leczone statynami obejmują nie tylko bolesność, ale również ogólny brak sił i chroniczne znużenie.
Wieloletnie poszukiwania odpowiedzi na pytanie o źródło tych problemów zakończyły się sukcesem, a zagadka kliniczna została ostatecznie rozwiązana.
Biologiczny mechanizm wycieku wapnia w komórkach
Badania opublikowane w „Journal of Clinical Investigation” przez zespół z Columbia University wskazują na konkretny mechanizm biologiczny odpowiedzialny za ból mięśni. Choć statyny mają za zadanie blokować enzym odpowiedzialny za syntezę cholesterolu, mogą one również oddziaływać na inne białka w organizmie.
Wykorzystując zaawansowaną metodę kriomikroskopii elektronowej, naukowcy zaobserwowali na poziomie atomowym interakcję simwastatyny z receptorem rianodynowym (RyR1), który reguluje przepływ jonów wapnia w mięśniach. Wykazano, że lek przyłącza się do białka RyR1 w dwóch miejscach, co powoduje rozszczelnienie kanału i niekontrolowany wyciek jonów wapnia do wnętrza komórki.
Prawidłowe funkcjonowanie włókien mięśniowych wymaga precyzyjnie regulowanego stężenia wapnia, dlatego jego nadmiar w niewłaściwych obszarach prowadzi do zaburzeń pracy mięśni. Taki stan aktywuje enzymy degradujące białka, co skutkuje bólem, osłabieniem, a nawet stopniowym uszkodzeniem tkanki. Autorzy badania zaznaczają jednak, że nie każda dolegliwość u pacjenta musi wynikać z tego konkretnego mechanizmu.
Perspektywy leczenia i nowe strategie farmakologiczne
Zrozumienie tego procesu stwarza realną szansę na spersonalizowane leczenie i uzupełnia brakujące ogniwo w wiedzy o działaniu statyn. Naukowcy wskazują dwie główne drogi ograniczenia działań niepożądanych u pacjentów.
Pierwsza strategia zakłada projektowanie nowych leków, które obniżą cholesterol bez wiązania się z receptorem RyR1, natomiast druga polega na farmakologicznym uszczelnieniu kanału wapniowego. Badania na myszach potwierdziły, że wyciek wapnia można zablokować eksperymentalną substancją opracowaną wcześniej do leczenia rzadkich schorzeń mięśniowych.
Obecnie trwają testy kliniczne tej substancji u ludzi w innych wskazaniach, co daje nadzieję na jej przyszłe wykorzystanie w leczeniu miopatii indukowanej statynami. Jeśli testy potwierdzą bezpieczeństwo i skuteczność preparatu, pacjenci cierpiący na bóle mięśniowe mogą zyskać nowe rozwiązanie terapeutyczne.
Skala problemu i rola nowoczesnej diagnostyki
Problemy z mięśniami odnotowywano od momentu wprowadzenia statyn na rynek pod koniec lat 80., a wcześniejsze hipotezy często wskazywały na interakcje z białkami. Przez lata brakowało jednak dowodów, które pozwoliłyby jednoznacznie potwierdzić te przypuszczenia.
Skala zjawiska jest znacząca, biorąc pod uwagę, że statyny przyjmuje kilkadziesiąt milionów osób, a objawy mięśniowe zgłasza około 10 procent z nich.
Dopiero rozwój technik obrazowania o wysokiej rozdzielczości pozwolił na wizualizację powiązań leków z białkami i wyjaśnienie konsekwencji tych procesów na poziomie komórkowym.
Źródło: PAP