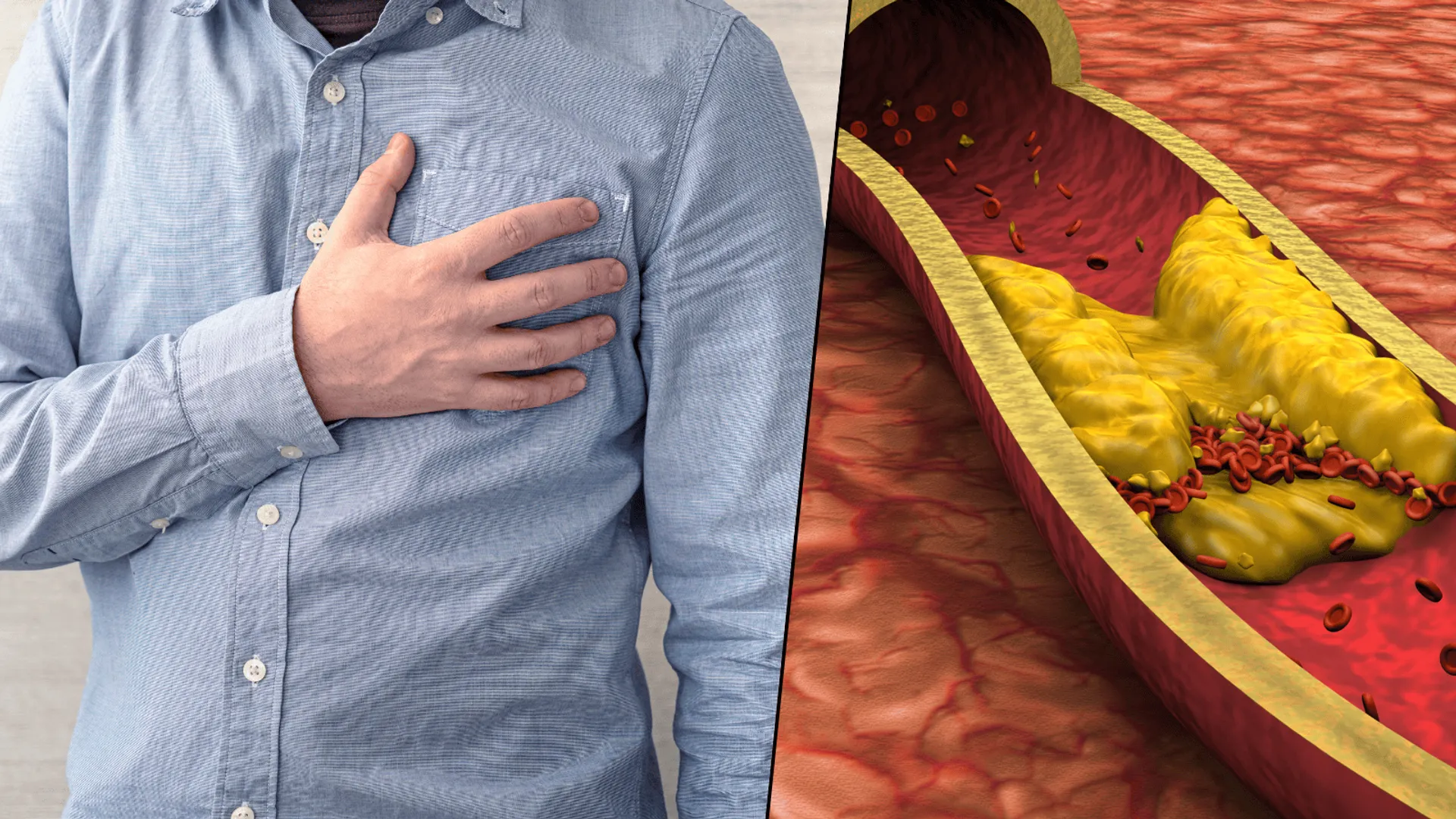
Główny Inspektor Farmaceutyczny podjął decyzję o natychmiastowym wycofaniu z obrotu leku Sunitinib MSN. Decyzja ta dotyczy jednej serii preparatu, stosowanego w terapii nowotworów, z powodu negatywnych wyników badań jakościowych przeprowadzonych przez Narodowy Instytut Leków. Stwierdzono nieszczelność kapsułek, co może prowadzić do wydostania się substancji czynnej i zakłócać precyzyjne dawkowanie leku.

Główny Inspektorat Farmaceutyczny wydał decyzję o natychmiastowym wycofaniu jednego z leków dla kobiet z obrotu w całej Polsce. Konkretna seria produktu musi zniknąć z aptek i hurtowni farmaceutycznych. Powodem są nieprawidłowości wykryte podczas badań jakościowych.

Sytuacja na Bliskim Wschodzie budzi obawy nie tylko w kontekście bezpieczeństwa międzynarodowego, ale także gospodarki i globalnych łańcuchów dostaw. Wśród pojawiających się pytań jest również to, czy eskalacja konfliktu może wpłynąć na dostępność leków w Polsce. Do sprawy odniósł się Główny Inspektorat Farmaceutyczny.

Główny Inspektorat Farmaceutyczny wydał pilną decyzję dotyczącą produktu stosowanego miejscowo na skórę. Z rynku w całej Polsce wycofano określone serie żelu stosowanego m.in. przy urazach i obrzękach. Decyzji nadano rygor natychmiastowej wykonalności, co oznacza, że preparat musi zostać niezwłocznie usunięty z aptek i nie może być dalej sprzedawany.

Główny Inspektorat Farmaceutyczny wydał pilny komunikat dotyczący jednego z produktów leczniczych dostępnych w polskich aptekach. Decyzja ta wiąże się z koniecznością natychmiastowego zaprzestania stosowania wskazanego preparatu przez pacjentów. Poniżej przedstawiamy szczegółowe informacje o przyczynach podjętych działań oraz zalecenia dla osób, które zakupiły ten środek. Chodzi o popularny lek wziewny.

Główny Inspektorat Farmaceutyczny poinformował o wykryciu sfałszowanego produktu sprzedawanego w aptekach ogólnodostępnych. Octenisept był przelewany do mniejszych, 50-mililitrowych butelek i oznaczany podrobionymi etykietami z numerami serii oraz datami ważności skopiowanymi z legalnych opakowań. Preparat konfekcjonowano poza autoryzowanym procesem i bez wymaganego nadzoru, co oznacza, że jego pochodzenie oraz bezpieczeństwo nie były gwarantowane.

Główny Inspektorat Sanitarny podjął decyzję o wycofaniu dwóch serii leków Sugammadex Reig Jofre na terenie całego kraju. Powód to wykrycie w roztworze widocznych cząsteczek silikonowych. Decyzja ma rygor natychmiastowej wykonalności.

Główny Inspektor Farmaceutyczny (GIF) podjął decyzję o wstrzymaniu sprzedaży popularnego leku przeciwbólowego. Jak się okazuje, partie środka nie spełniają ustalonych wymagań jakościowych. Chodzi dokładnie o lek Ibuprofen Dr. Max.To popularny lek przeciwbólowy i przeciwzapalny należący do grupy leków nazywanych NLPZ - niesteroidowe leki przeciwzapalne, działające poprzez zmniejszenie bólu, gorączki oraz stanu zapalnego. Stosuje się go w krótkotrwałym leczeniu bólu o nasileniu łagodnym i umiarkowanym.