Natychmiastowa decyzja GIF: tabletki z miodem i cytryną na ból gardła wycofane ze sprzedaży
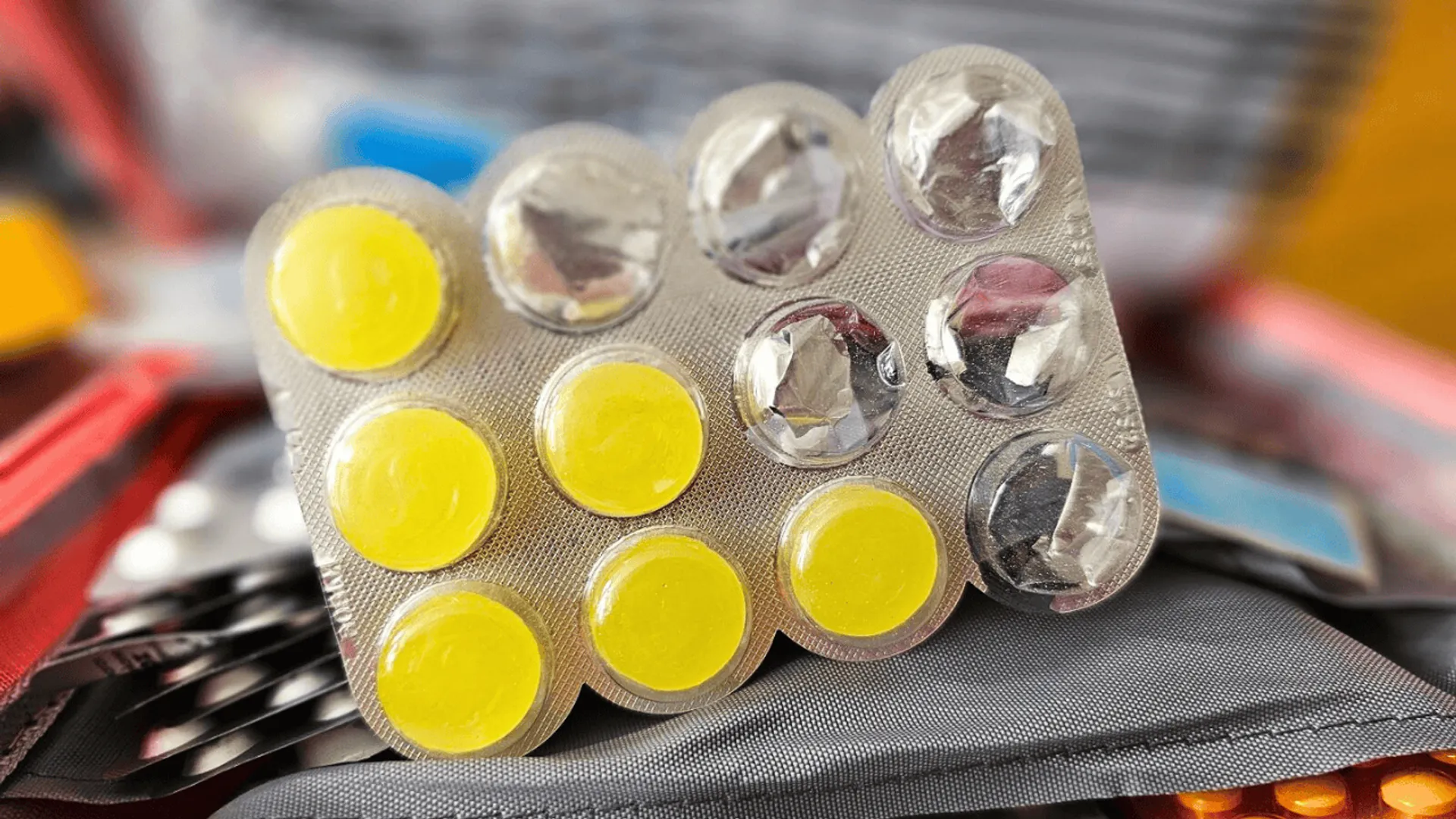
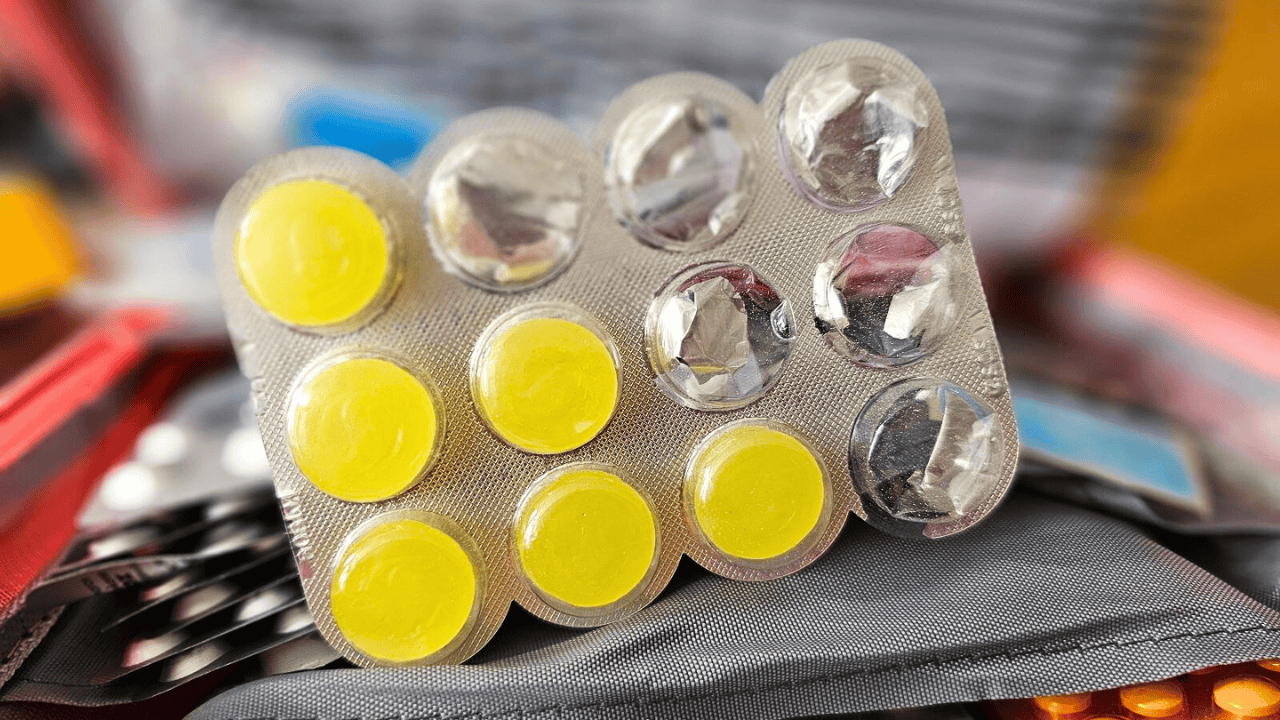
Tabletki na ból i infekcje gardła Strepsils z miodem i cytryną w całej Polsce zostały wycofane ze sprzedaży. Jak podaje Główny Inspektorat Farmaceutyczny, seria produktu została zanieczyszczona substancją o nieznanym pochodzeniu, powodując ryzyko wystąpienia nieprzewidywalnych konsekwencji medycznych.
Ze względu na zdrowie pacjentów, decyzja została nadana pod rygorem natychmiastowej wykonalności. Z obrotu została wycofana jedna seria leku.
Sprawdź, czy nie masz w apteczce
Strepsils to popularne pastylki stosowane na ból gardła, o działaniu antyseptycznym, zwalczającym wirusy i bakterie. Dostępny jest w aptekach i sklepach spożywczych w całej Polsce.
Według GIF: „Zanieczyszczenie produktu leczniczego substancją o nieznanym pochodzeniu i charakterze stwarza realne ryzyko wystąpienia, niedających się przewidzieć konsekwencji medycznych”. W trosce o zdrowie i życie pacjentów, którzy stosowaliby produkt niespełniający wymagań jakościowych, decyzja o wycofaniu tabletek z obrotu była uzasadniona i konieczna. Nadano jej rygor natychmiastowej wykonalności.
Produkt kupiony w sklepie spożywczym
Jak podano w uzasadnieniu, do „Głównego Inspektora Farmaceutycznego wpłynęło zgłoszenie pacjenta dotyczące podejrzenia braku spełnienia wymagań jakościowych produktu leczniczego Strepsils z miodem i cytryną (…)”. Strepsils to produkt leczniczy wydawany bez recepty. Tabletki zostały kupione w jednej z sieci sklepów spożywczych. Pochodzenie i charakter zanieczyszczenia są nieznane, a innych zgłoszeń tego typu nie otrzymano.
Produkt wycofany przez Główny Inspektorat Farmaceutyczny
Pastylki twarde Strepsils z miodem i cytryną (Alcohol 2,4-dichlorobenzylicus + Amylmetacresolum)
Opakowanie 12 sztuk 1,2 mg + 0,6 mg, GTIN 05909990192434
Numer serii: RT019
Termin ważności: 30.11.2026 r.
Wytwórcą produktu jest Reckitt Benckiser Healthcare International Ltd z siedzibą w Wielkiej Brytanii , podmiot odpowiedzialny: Reckitt Benckiser (Poland) S.A. z siedzibą w Nowym Dworze Mazowieckim
W podsumowaniu uzasadnienia podano, że „decyzja ma charakter zabezpieczający i służy wstrzymaniu obrotu produktem leczniczym, co do jakości którego istnieje uzasadnione podejrzenia, na czas przeprowadzenia dalszego postępowania wyjaśniającego”.
Źródło:
Czytaj także:
Jesienią dzieci chorują częściej. Jak przygotować apteczkę, by nie dać się zaskoczyć infekcji?
Dziecku leci krew z nosa? Pediatra tłumaczy, dlaczego czasem tak się dzieje
Matka wcześnie zauważyła pierwsze objawy choroby syna. Trzy lata po diagnozie, dziecko zmarło