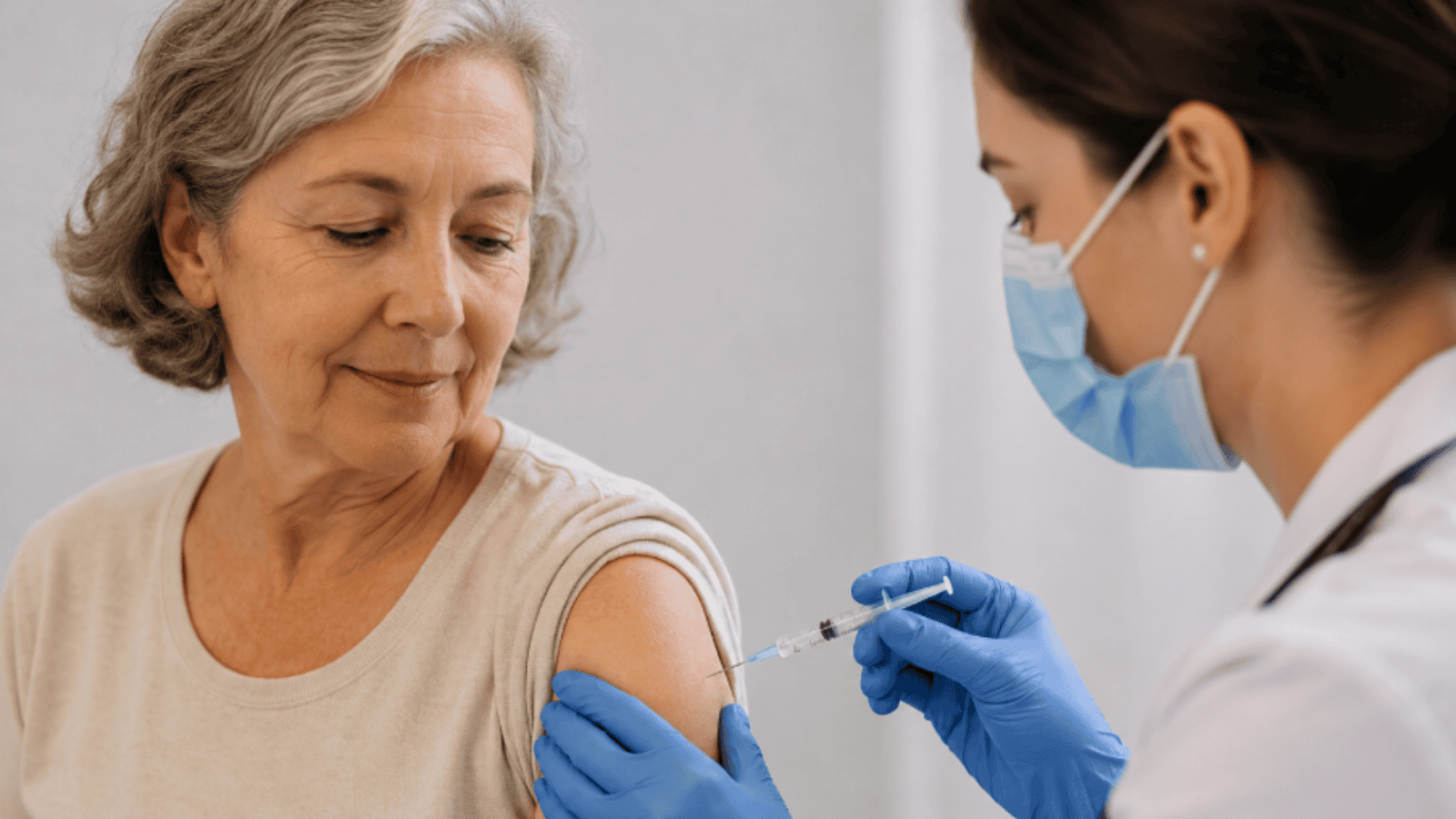
Nowa szczepionka mRNA przeciw grypie znacznie skuteczniejsza. Szczegółowe wyniki badań
Firma Moderna potwierdziła wysoką skuteczność profilaktyczną swojej sezonowej szczepionki przeciw grypie opartej na technologii mRNA. Publikacja wyników badań klinicznych w czasopiśmie New England Journal of Medicine wykazała przewagę nowego preparatu nad dotychczas stosowanymi standardowymi szczepionkami. Amerykańska Agencja Żywności i Leków (FDA), po wcześniejszej odmowie i związanych z nią obiekcjach metodologicznych, wyznaczyła termin ostatecznej decyzji o dopuszczeniu preparatu na rynek na sierpień 2026 roku.
- Szczepionka mRNA-1010 wykazała względną skuteczność na poziomie 26,6 procent w całej populacji badawczej oraz 27,4 procent u osób powyżej 65. roku życia
- Występowanie zdarzeń niepożądanych, takich jak ból w miejscu wkłucia czy zmęczenie, było wyższe w przypadku technologii mRNA w porównaniu z klasycznymi preparatami
- FDA zmieniła swoją pierwotną decyzję o odrzuceniu wniosku rejestracyjnego i podejmie ostateczną decyzję na mocy ustawy PDUFA do 5 sierpnia 2026 roku
Skuteczność preparatu mRNA-1010 i wyniki badania III fazy
Firma Moderna ogłosiła szczegółowe wyniki badania klinicznego III fazy o akronimie NCT06602024, oceniającego szczepionkę przeciw grypie sezonowej opartą na technologii kwasu rybonukleinowego. Analiza, którą opublikowano w recenzowanym czasopiśmie naukowym New England Journal of Medicine, opiera się na danych uzyskanych od ponad 40 tysięcy dorosłych pacjentów w wieku powyżej 50 lat. Zebrany materiał badawczy pochodzi z monitorowania pacjentów podczas sezonu infekcyjnego 2024–2025.
Wyniki udowodniły statystyczną przewagę preparatu mRNA-1010 nad licencjonowanymi szczepionkami w standardowej dawce, w tym komparatorem Fluarix produkcji firmy GSK. Analitycy zarejestrowali względną skuteczność szczepionki wynoszącą 26,6 procent w pełnej grupie uczestników. U osób w wieku 65 lat i starszych, które ze względu na wiek tworzą grupę podwyższonego ryzyka ciężkiego przebiegu choroby, parametr skuteczności ukształtował się na zbliżonym poziomie 27,4 procent.
Zdolność neutralizacji wirusa różniła się w zależności od docelowego szczepu patogenu. Ochrona przed linią A/H1N1 wyniosła 29,6 procent, w odniesieniu do A/H3N2 osiągnęła 22,2 procent, natomiast dla linii B/Victoria wskaźnik skuteczności wyniósł 29,1 procent. W odniesieniu do weryfikacji tych statystyk stanowisko zajął dyrektor generalny firmy Moderna, Stéphane Bancel:
– Publikacja tych poddanych recenzji, pozytywnych wyników w New England Journal of Medicine odzwierciedla siłę dowodów klinicznych wspierających nasze trwające wnioski rejestracyjne.
Zwiększona ochrona immunologiczna oferowana przez platformę mRNA łączyła się jednocześnie z częstszym raportowaniem odczynów poszczepiennych względem tradycyjnych szczepionek z białkiem rekombinowanym lub inaktywowanym wirusem. Główne różnice w profilu bezpieczeństwa zdefiniowano w następujących kategoriach:
- ból w miejscu iniekcji odnotowano u 65,8 procent osób badanych wobec 29,8 procent w grupie otrzymującej komparator,
- ogólne zmęczenie organizmu zgłosiło 45,1 procent zaszczepionych preparatem Moderny w zestawieniu z 20,3 procent po tradycyjnej dawce,
- bóle głowy wystąpiły u 37,8 procent pacjentów po szczepionce mRNA w porównaniu do 18,0 procent w grupie kontrolnej.
Kontrowersje regulacyjne i zmiana stanowiska Agencji Żywności i Leków (FDA)
Ścieżka certyfikacji preparatu mRNA-1010 na terytorium Stanów Zjednoczonych uległa znacznemu wydłużeniu na skutek decyzji organów nadzorczych. W pierwszej instancji Amerykańska Agencja Żywności i Leków (FDA) kategorycznie odmówiła procedowania wniosku o rejestrację produktu. Podstawą tej odmowy był zarzut braku zaimplementowania adekwatnego modelu porównawczego w kohorcie pacjentów geriatrycznych, co wywołało konfrontację między producentem a organem regulacyjnym.
Podłożem konfliktu metodologicznego był dobór dawki w szczepionce porównawczej dla osób po 65. roku życia. Zgodnie z oficjalnymi wytycznymi Komitetu Doradczego ds. Praktyk Szczepień (ACIP), preferowanym standardem medycznym dla tej grupy demograficznej są preparaty zawierające wysoką dawkę antygenu. Firma Moderna wykorzystała w swoim badaniu wariant o dawce standardowej. Rygorystyczne stanowisko administracji wyartykułował rzecznik Departamentu Zdrowia i Opieki Społecznej Stanów Zjednoczonych (HHS), Andrew Nixon:
– Moderna naraziła uczestników w wieku 65 lat i starszych na zwiększone ryzyko ciężkiej choroby, podając im standard opieki niższy niż zalecany przez naukowców FDA.
Mimo surowej krytyki, po przedstawieniu przez producenta dodatkowych danych klinicznych, FDA zdecydowała się na zmianę stanowiska i przyjęła zmodyfikowany wniosek biologiczny (BLA) do merytorycznej ewaluacji. Wypracowany kompromis regulacyjny rozdziela tryb akceptacji na dwie kategorie wiekowe: firma oczekuje pełnego zatwierdzenia dla populacji w przedziale 50–64 lata oraz przyspieszonego zatwierdzenia dla osób powyżej 65 lat. Datę ogłoszenia werdyktu wyznaczono na 5 sierpnia 2026 roku.
Znaczenie technologii mRNA dla przyszłości rynku szczepionek
Decyzja amerykańskiego regulatora zdeterminuje trajektorię rozwoju profilaktyki schorzeń układu oddechowego na nadchodzące lata. Integracja rozwiązań genetycznych w sezonowych programach ochronnych zmusza rynek do modyfikacji dotychczasowych modeli biznesowych i medycznych. Skalę rynkowego potencjału nowej technologii podsumowała Stephanie Kurdach, analityczka specjalizująca się w chorobach zakaźnych z ramienia instytucji badawczej GlobalData:
– Szczepionki oparte na technologii mRNA, takie jak mRNA-1010, mogą stanowić ogromny postęp dla rynku szczepionek przeciw grypie sezonowej.
Zasadniczą wartością operacyjną technologii mRNA w kontekście grypy sezonowej jest ominięcie czasochłonnej fazy hodowli w zarodkach kurzych. Pozwala to na drastyczne skrócenie cyklu produkcyjnego, co umożliwia laboratoriom znacznie precyzyjniejsze dopasowanie genetyczne szczepionki do konkretnych wariantów patogenu krążących w danym środowisku tuż przed rozpoczęciem fali zachorowań.
Podczas gdy dyskusje metodologiczne wewnątrz amerykańskich instytucji federalnych wstrzymały wdrożenie preparatu w USA, ekspansja międzynarodowa pozostaje w toku. Wnioski o dopuszczenie szczepionki mRNA-1010 do obrotu medycznego są aktywnie weryfikowane przez Europejską Agencję Leków (EMA). Analogiczne procedury sprawdzające prowadzą niezależnie urzędy do spraw bezpieczeństwa farmakoterapii w Australii oraz w Kanadzie, co pozwoli ustabilizować nową architekturę zabezpieczeń epidemicznych na poziomie globalnym.
Źródło: Pacjenci.pl