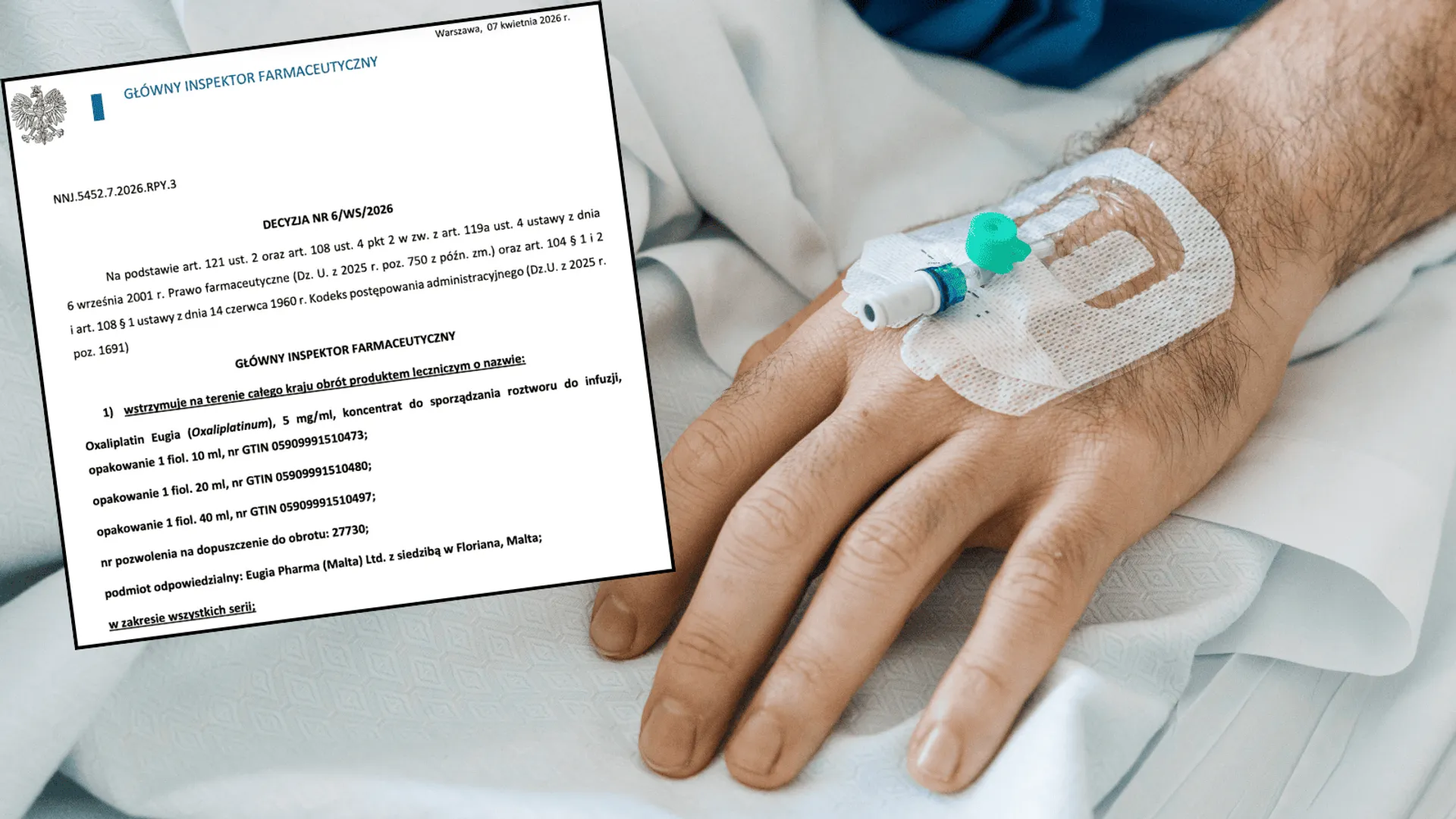
To wiadomość, która uderza prosto w serce tysięcy polskich rodzin walczących z chorobą nowotworową. Główny Inspektorat Farmaceutyczny (GIF) wydał 7 kwietnia 2026 r. decyzję o natychmiastowym wstrzymaniu obrotu lekiem Oxaliplatin Eugia, stosowanym w chemioterapii. W preparacie, który trafia prosto do krwiobiegu pacjentów, wykryto zanieczyszczenia mechaniczne widoczne gołym okiem.Dowiedz się, dlaczego GIF wstrzymał wszystkie serie tego lekuSprawdź, co dokładnie wykryły badania Narodowego Instytutu LekówJakie kroki musisz podjąć, jeśli Ty lub Twój bliski przyjmujecie ten preparat?

Bezpieczeństwo zdrowotne to priorytet, a skuteczność terapii zależy bezpośrednio od jakości stosowanych preparatów. W marcu i kwietniu 2026 roku Główny Inspektorat Farmaceutyczny (GIF) wydał szereg rygorystycznych decyzji o wycofaniu oraz wstrzymaniu obrotu popularnych leków. Wśród nich znalazły się preparaty na astmę, silne stany lękowe, bóle mięśni, a nawet środki stosowane w chemioterapii.Gdy leki nie spełniają rygorystycznych norm jakościowych (np. mają nieodpowiednią dawkę, mniejszą objętość w ampułce lub widoczne zanieczyszczenia), ich przyjmowanie może stanowić bezpośrednie zagrożenie dla Twojego zdrowia lub skutkować całkowitym brakiem efektów leczenia.Oto rzetelne zestawienie leków zakwestionowanych przez GIF w ostatnich tygodniach. Sprawdź swoją domową apteczkę.

Bezpieczeństwo pacjentów poddawanych specjalistycznej diagnostyce zostało wystawione na poważną próbę. Główny Inspektor Farmaceutyczny wydał dwie natychmiastowe decyzje o wycofaniu z obrotu w całym kraju serii produktów. Powodem tej radykalnej interwencji jest wykrycie zanieczyszczenia, które bezpośrednio zagraża zdrowiu i życiu pacjentow. Wykryte ciała obce wymusiły natychmiastowe wstrzymanie dystrybucji i sprzedaży.Mechaniczne zanieczyszczenie partii produkcyjnychSzczegółowe zestawienie wycofanych produktów i seriiPostępowanie w placówkach medycznych i diagnostycznych

Główny Inspektor Farmaceutyczny wydał pilną decyzję o wycofaniu z obrotu na terenie całego kraju partii leku stosowanego u najmłodszych pacjentów. Powodem tej radykalnej decyzji jest ryzyko wystąpienia skażenia mikrobiologicznego, które wykryto podczas wewnętrznych kontroli producenta. Sprawa jest poważna, ponieważ preparat trafia bezpośrednio do układu oddechowego noworodków, co wymaga zachowania najwyższych standardów sterylności.Przyczyny decyzji Głównego Inspektora FarmaceutycznegoZastosowanie i działanie preparatu u noworodkówZagrożenia wynikające z zanieczyszczenia lekuSzczegółowe dane wycofanych serii produktu

Główny Inspektor Farmaceutyczny podjął decyzję o natychmiastowym wycofaniu z obrotu leku Sunitinib MSN. Decyzja ta dotyczy jednej serii preparatu, stosowanego w terapii nowotworów, z powodu negatywnych wyników badań jakościowych przeprowadzonych przez Narodowy Instytut Leków. Stwierdzono nieszczelność kapsułek, co może prowadzić do wydostania się substancji czynnej i zakłócać precyzyjne dawkowanie leku.

Główny Inspektor Farmaceutyczny wydał pilną decyzję o wstrzymaniu obrotu popularnym lekiem stosowanym w poważnych schorzeniach autoimmunologicznych. Powodem jest podejrzenie wady jakościowej, która może zagrażać bezpieczeństwu pacjentów przyjmujących ten preparat. Podczas rutynowych badań stabilności wykryto niepokojące zmiany mikrobiologiczne, co w przypadku leków do wstrzykiwań stanowi poważny problem.Przyczyny wstrzymania leku przez inspektoratZastosowanie preparatu oraz dane konkretnych seriiPostępowanie dla pacjentów posiadających lek

Główny Inspektorat Farmaceutyczny wydał decyzję o natychmiastowym wycofaniu jednego z leków dla kobiet z obrotu w całej Polsce. Konkretna seria produktu musi zniknąć z aptek i hurtowni farmaceutycznych. Powodem są nieprawidłowości wykryte podczas badań jakościowych.

Sytuacja na Bliskim Wschodzie budzi obawy nie tylko w kontekście bezpieczeństwa międzynarodowego, ale także gospodarki i globalnych łańcuchów dostaw. Wśród pojawiających się pytań jest również to, czy eskalacja konfliktu może wpłynąć na dostępność leków w Polsce. Do sprawy odniósł się Główny Inspektorat Farmaceutyczny.

Główny Inspektorat Farmaceutyczny wydał pilną decyzję dotyczącą produktu stosowanego miejscowo na skórę. Z rynku w całej Polsce wycofano określone serie żelu stosowanego m.in. przy urazach i obrzękach. Decyzji nadano rygor natychmiastowej wykonalności, co oznacza, że preparat musi zostać niezwłocznie usunięty z aptek i nie może być dalej sprzedawany.

Główny Inspektor Farmaceutyczny wydał pilny komunikat dotyczący wycofania z obrotu popularnego preparatu stosowanego w stanach podgorączkowych oraz przy dolegliwościach bólowych u dzieci. Decyzja ma rygor natychmiastowej wykonalności, co oznacza, że produkt musi zniknąć z półek aptecznych w całym kraju bez żadnej zwłoki. Rodzice powinni jak najszybciej przejrzeć zawartość swoich domowych apteczek, aby upewnić się, że nie posiadają wadliwej partii leku.Przyczyny decyzji Głównego Inspektora FarmaceutycznegoSzczegółowe dane wycofanej serii produktuInstrukcja postępowania dla rodziców i opiekunów

Główny Inspektorat Farmaceutyczny wydał pilny komunikat dotyczący jednego z produktów leczniczych dostępnych w polskich aptekach. Decyzja ta wiąże się z koniecznością natychmiastowego zaprzestania stosowania wskazanego preparatu przez pacjentów. Poniżej przedstawiamy szczegółowe informacje o przyczynach podjętych działań oraz zalecenia dla osób, które zakupiły ten środek. Chodzi o popularny lek wziewny.

Luty 2026 roku przyniósł serię pilnych komunikatów Głównego Inspektoratu Farmaceutycznego (GIF). Urząd wydał kilka decyzji o wycofaniu z obrotu produktów, które cieszą się dużą popularnością i często trafiają do naszych domowych apteczek. Niektóre z tych rozstrzygnięć otrzymały rygor natychmiastowej wykonalności. Oznacza to, że wskazanych partii nie wolno stosować pod żadnym pozorem, a ich dalsza sprzedaż została zabroniona. Warto poświęcić chwilę na przegląd zapasów, aby zadbać o bezpieczeństwo swoje i najbliższych.Grofibrat 200 wycofany w trybie natychmiastowymLoperamid APTEO MED znika z rynkuProblemy z jakością leku LorafenZanieczyszczenia w ampułkach kwasu traneksamowegoSfałszowany Octenisept w obieguPrawidłowe postępowanie z wycofanym lekiem

Główny Inspektorat Farmaceutyczny poinformował o wykryciu sfałszowanego produktu sprzedawanego w aptekach ogólnodostępnych. Octenisept był przelewany do mniejszych, 50-mililitrowych butelek i oznaczany podrobionymi etykietami z numerami serii oraz datami ważności skopiowanymi z legalnych opakowań. Preparat konfekcjonowano poza autoryzowanym procesem i bez wymaganego nadzoru, co oznacza, że jego pochodzenie oraz bezpieczeństwo nie były gwarantowane.

Główny Inspektor Farmaceutyczny wydał pilną decyzję o wycofaniu z obrotu popularnego preparatu stosowanego przez pacjentów zmagających się z wysokim poziomem lipidów we krwi. Urzędnicy nadali decyzji rygor natychmiastowej wykonalności, co oznacza, że produkt musi zniknąć z aptek w całym kraju w trybie pilnym. Przyczyną radykalnego kroku są wyniki badań, które podważyły jakość jednej z partii leku, co może bezpośrednio wpływać na efekty prowadzonej terapii.Decyzja o natychmiastowym wycofaniu z aptek popularnego lekuZagrożenie dla zdrowia wynikające z braku skuteczności terapiiWyniki szczegółowego dochodzenia przeprowadzonego przez producentaO jaki lek chodzi w komunikacie GIF?

Główny Inspektorat Farmaceutyczny (GIF) wydał pilny komunikat dotyczący wycofania z obrotu popularnego leku stosowanego przy dolegliwościach układu pokarmowego. Decyzja ma rygor natychmiastowej wykonalności, co oznacza, że produkt musi natychmiast zniknąć z aptecznych półek w całym kraju. Powodem interwencji jest wykryta wada jakościowa, która może bezpośrednio rzutować na proces leczenia pacjentów.Przyczyny decyzji i wyniki badań stabilnościRygor natychmiastowej wykonalności i jego konsekwencjeInstrukcja postępowania dla pacjentówSzczegółowe dane wycofanej partii leku

Krajowy organ nadzorczy wydał natychmiastową decyzję o wycofaniu z obrotu popularnego preparatu przepisywanego pacjentom zmagającym się z silnymi stanami lękowymi oraz zaburzeniami snu. Powodem interwencji jest wykryta wada jakościowa, która mogła powstać w procesie produkcyjnym i realnie wpływać na skuteczność terapii. Osoby stosujące ten rodzaj leczenia powinny niezwłocznie sprawdzić numery serii posiadanych opakowań, gdyż wadliwe tabletki nie gwarantują odpowiedniego działania substancji czynnej.Przyczyna decyzji Głównego Inspektora FarmaceutycznegoRyzyko dla zdrowia i rygor natychmiastowej wykonalnościSzczegółowe dane wycofanego produktuCo powinni zrobić pacjenci posiadający wadliwe serie

Główny Inspektor Farmaceutyczny poinformował o wycofaniu z rynku popularnego płynu odkażającego. Decyzja ma rygor natychmiastowej wykonalności. Chodzi o jeden z powszechnie stosowanych preparatów do odkażania błon śluzowych. Powodem są wątpliwości dotyczące jego jakości, które – jak podkreśla inspektorat – mogą stanowić realne zagrożenie dla zdrowia pacjentów.Co wzbudziło niepokój inspektorów i dlaczego podjęto pilną decyzję?Z używaniem wadliwego preparatu wiąże się poważne ryzykoO jaki dokładnie produkt chodzi w komunikacie GIF?

Decyzja zapadła natychmiast i objęła całą Polskę. Inspekcja farmaceutyczna zdecydowała o wycofaniu z obrotu preparatu stosowanego u pacjentów z ciężkimi zaburzeniami psychicznymi. Powód? Poważne nieprawidłowości wykryte w procesie produkcji i realne zagrożenie dla zdrowia.Zagraniczna kontrola uruchomiła alarm w PolsceZastrzyk, który może zaszkodzić zamiast pomócO jaki lek chodzi w komunikacie GIF?

Bezpieczeństwo najmłodszych konsumentów jest priorytetem, dlatego wszelkie sygnały o możliwych nieprawidłowościach wymagają natychmiastowej reakcji. Poniższa informacja dotyczy ostrożnościowych działań podjętych w celu wyeliminowania potencjalnego ryzyka związanego z określoną grupą produktów do żywienia niemowląt.

Popularna sieć sklepów wystosowała pilny komunikat dotyczący bezpieczeństwa jednego z produktów sportowych. Klienci, którzy nabyli konkretny model akcesoriów treningowych, powinni natychmiast zaprzestać jego użytkowania. Poniżej przedstawiamy szczegóły dotyczące identyfikacji wadliwego towaru oraz instrukcję zwrotu dla konsumentów.

Główny Inspektor Farmaceutyczny wydał pilną decyzję o wycofaniu z obrotu jednego z często stosowanych antybiotyków. Preparat zniknął z aptek w całej Polsce, a decyzji nadano rygor natychmiastowej wykonalności. Powodem wycofania są poważne wątpliwości dotyczące jakości substancji.Decyzja GIF obowiązuje w całym kraju i działa natychmiastTen antybiotyk trafił na listę wycofanych – sprawdź dokładne daneJakość substancji czynnej przesądziła o wycofaniu leku z rynku

W Zespole analizującym przepływów finansowych w systemie ochrony zdrowia doszło do istotnej zmiany. Zgodnie z najnowszym zarządzeniem Ministra Zdrowia, funkcję przewodniczącego tego gremium obejmuje Łukasz Pietrzak – Główny Inspektor Farmaceutyczny. Kim jest i jaki ma dorobek? Wyjaśniamy.Nowe przepisy opublikowano w Dzienniku Urzędowym Ministra Zdrowia. Chodzi o Zarządzenie Ministra Zdrowia z 12 grudnia 2025 r. (poz. 97), które zmienia regulacje dotyczące powołania Zespołu do spraw analizy przepływów finansowych przeznaczonych na ochronę zdrowia. Najważniejsza zmiana personalna to właśnie powierzenie kierownictwa Zespołu Łukaszowi Pietrzakowi.Jednocześnie obsługę organizacyjno-techniczną Zespołu przejął Główny Inspektorat Farmaceutyczny. Oznacza to formalne przesunięcie ciężaru koordynacji analiz finansowych na instytucję odpowiedzialną za nadzór nad rynkiem leków.
Rośnie liczba leków, które mogą być szkodliwe - Główny Inspektor Farmaceutyczny prowadzi szerokie kontrole i w razie wystąpienia jakichkolwiek nieprawidłowości od razu podejmuje decyzję o wycofaniu danych preparatów z obrotu. Zdrowie konsumentów i ich bezpieczeństwo są tu najważniejsze. W grudniu, choć mamy ledwo połowę miesiąca, już doszło do wycofania kilku leków, dość popularnych. Lepiej sprawdź swoją apteczkę.

Picie dobrej wody to nie tylko gaszenie pragnienia — to element codziennej profilaktyki zdrowotnej. Dlatego tak istotne jest, że Główny Inspektorat Sanitarny (GIS) opublikował najnowszy wykaz naturalnych wód mineralnych w Polsce, czyli tych, które spełniają najbardziej rygorystyczne normy czystości i bezpieczeństwa.W 2025 roku lista została zaktualizowana na podstawie szczegółowych badań źródła i składu chemicznego. Znalazło się na niej 119 wód, które mogą być oficjalnie uznawane za naturalne mineralne — a więc jedne z najbezpieczniejszych i najbardziej kontrolowanych produktów dostępnych na rynku.Kryteria obejmują m.in. czystość środowiskową ujęcia, stabilną i odpowiednią zawartość minerałów oraz niską zawartość zanieczyszczeń. Wszystkie badania wykonują uprawnione laboratoria.

Chorzy w Polsce znów stają przed realnym ryzykiem: GIF opublikował kolejną listę leków zagrożonych brakiem dostępności. Dla wielu pacjentów oznacza to niepewność, czy otrzymają potrzebny preparat dokładnie wtedy, gdy będzie najbardziej potrzebny. Lista leków o utrudnionej dostępności obejmuje setki produktów i w ostatnich latach systematycznie się wydłuża. Przyczyn jest wiele — od zakłóceń w łańcuchu produkcji i dystrybucji, przez gwałtowny wzrost popytu, po eksport leków za granicę, który wymusza dodatkowe działania nadzorcze państwa.Problemy dotyczą różnych grup leków: antybiotyków, preparatów neurologicznych, leków onkologicznych oraz podstawowych terapii stosowanych przewlekle. Każdy z tych segmentów reaguje na inne zjawiska rynkowe, ale skutki dla pacjentów są podobne — niepewność i konieczność dostosowania leczenia.

Główny Inspektorat Farmaceutyczny poinformował o wycofaniu z obrotu kilku leków i kropli do oczu. Decyzje zapadły na podstawie wykrytych nieprawidłowości związanych z jakością i bezpieczeństwem preparatów. Chodzi m.in. o zanieczyszczenia chemiczne, niewłaściwe uwalnianie substancji czynnych oraz przekroczenia dopuszczalnych norm zawartości składników aktywnych.GIF wycofał z aptek popularne leki i krople do oczu – sprawdź listę i numery seriiSprawdź, które leki zostały wycofane przez GIF w listopadzie 2025 i co zrobić, jeśli masz je w domuLista wycofanych leków i kropli do oczu: decyzje GIF, powody i zalecenia dla pacjentów

Polacy połykają leki i suplementy w ogromnych ilościach — często bez refleksji, bez konsultacji i bez czytania ulotki. Tymczasem rośnie liczba zatruć, zwłaszcza wśród młodszych pacjentów. Główny Inspektorat Farmaceutyczny reaguje i dołącza do kampanii, która ma zatrzymać ten niebezpieczny trend.
Główny Inspektor Farmaceutyczny nakazał natychmiastowe wycofanie z aptek wybranych serii popularnych kropli do oczu stosowanych w leczeniu jaskry. Powodem są wykryte nieprawidłowości, które mogą wpływać zarówno na bezpieczeństwo, jak i skuteczność leczenia.Wycofanie dotyczy leku stosowanego na receptę w terapii jaskry i nadciśnienia wewnątrzgałkowegoW części serii wykryto parametry mogące podrażniać powierzchnię oka. W innych – zaniżoną objętość, co oznacza, że pacjent mógł otrzymać mniej leku, niż deklaruje producentGIF nadał decyzji rygor natychmiastowej wykonalnościPacjenci powinni sprawdzić numery serii w domowych apteczkach